Theoretische Diskussion zum Aerosolstabilitätstest, der durch die Arrhenius-Formel induziert wird
Der notwendige Prozess für die Markteinführung unserer Aerosolprodukte ist die Durchführung eines Stabilitätstests. Wir werden jedoch feststellen, dass es trotz bestandener Stabilitätstests immer noch zu unterschiedlichen Graden von Korrosionslecks in der Massenproduktion oder sogar zu Qualitätsproblemen bei Massenprodukten kommt.Ist es für uns also immer noch sinnvoll, einen Stabilitätstest durchzuführen?
Normalerweise sprechen wir von 50℃. Drei Monate Stabilitätstest entsprechen zwei Jahren theoretischem Testzyklus bei Raumtemperatur. Woher kommt also der theoretische Wert?Eine bemerkenswerte Formel muss hier erwähnt werden: die Arrhenius-Formel.Die Arrhenius-Gleichung ist ein chemischer Begriff.Es handelt sich um eine empirische Formel für die Beziehung zwischen der Geschwindigkeitskonstante einer chemischen Reaktion und der Temperatur.Viel Praxis zeigt, dass diese Formel nicht nur auf Gasreaktionen, Flüssigphasenreaktionen und die meisten mehrphasigen katalytischen Reaktionen anwendbar ist.
Formelschreiben (exponentiell)
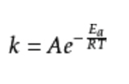
K ist die Geschwindigkeitskonstante, R ist die molare Gaskonstante, T ist die thermodynamische Temperatur, Ea ist die scheinbare Aktivierungsenergie und A ist der präexponentielle Faktor (auch als Frequenzfaktor bekannt).
Es ist zu beachten, dass die empirische Formel von Arrhenius davon ausgeht, dass die Aktivierungsenergie Ea als eine von der Temperatur unabhängige Konstante betrachtet wird, was mit experimentellen Ergebnissen innerhalb eines bestimmten Temperaturbereichs übereinstimmt.Aufgrund eines großen Temperaturbereichs oder komplexer Reaktionen sind LNK und 1/T jedoch keine gute Gerade.Es zeigt, dass die Aktivierungsenergie mit der Temperatur zusammenhängt und die empirische Formel von Arrhenius auf einige komplexe Reaktionen nicht anwendbar ist.
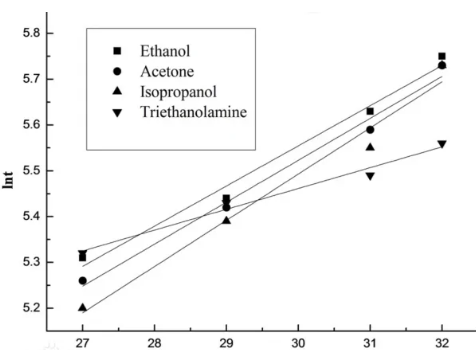
Können wir der empirischen Formel von Arrhenius in Aerosolen noch folgen?Abhängig von der Situation werden die meisten davon bis auf wenige Ausnahmen befolgt, vorausgesetzt natürlich, dass die „Aktivierungsenergie Ea“ des Aerosolprodukts eine stabile, temperaturunabhängige Konstante ist.
Zu seinen chemischen Einflussfaktoren zählen nach der Arrhenius-Gleichung folgende Aspekte:
(1) Druck: Bei chemischen Reaktionen mit Gasen wird der Druck erhöht, wenn andere Bedingungen (außer dem Volumen) unverändert bleiben, d effektive Kollisionen pro Zeiteinheit nehmen zu und die Reaktionsgeschwindigkeit beschleunigt sich;Andernfalls nimmt es ab.Bei konstantem Volumen bleibt die Reaktionsgeschwindigkeit bei Druck konstant (durch Zugabe eines Gases, das nicht an der chemischen Reaktion teilnimmt).Da sich die Konzentration nicht ändert, ändert sich auch die Anzahl der aktiven Moleküle pro Volumen nicht.Aber wenn man bei konstantem Volumen die Reaktanten hinzufügt, wiederum Druck ausübt und die Konzentration der Reaktanten erhöht, erhöht sich die Geschwindigkeit.
(2) Temperatur: Solange die Temperatur erhöht wird, gewinnen die Reaktantenmoleküle Energie, so dass ein Teil der ursprünglich energiearmen Moleküle zu aktivierten Molekülen wird, wodurch der Prozentsatz der aktivierten Moleküle zunimmt und die Anzahl der effektiven Kollisionen zunimmt, sodass die Reaktion abläuft Tariferhöhungen (der Hauptgrund).Durch den Temperaturanstieg wird natürlich die Geschwindigkeit der molekularen Bewegung beschleunigt und die Anzahl der molekularen Kollisionen der Reaktanten pro Zeiteinheit erhöht, und die Reaktion wird entsprechend beschleunigt (sekundäre Ursache).
(3) Katalysator: Durch die Verwendung eines positiven Katalysators kann die für die Reaktion erforderliche Energie reduziert werden, sodass mehr Reaktantenmoleküle zu aktivierten Molekülen werden, wodurch der Prozentsatz der Reaktantenmoleküle pro Volumeneinheit erheblich verbessert und somit die Reaktantenrate tausendfach erhöht wird.Negativer Katalysator ist das Gegenteil.
(4) Konzentration: Wenn andere Bedingungen gleich sind, erhöht eine Erhöhung der Konzentration der Reaktanten die Anzahl der aktivierten Moleküle pro Volumeneinheit, wodurch die effektive Kollision erhöht wird, die Reaktionsgeschwindigkeit steigt, aber der Prozentsatz der aktivierten Moleküle bleibt unverändert.
Die chemischen Faktoren aus den oben genannten vier Aspekten können unsere Klassifizierung von Korrosionsstellen (Gasphasenkorrosion, Flüssigphasenkorrosion und Grenzflächenkorrosion) gut erklären:
1) Bei der Gasphasenkorrosion bleibt das Volumen zwar unverändert, der Druck steigt jedoch an.Mit steigender Temperatur nimmt die Aktivierung von Luft (Sauerstoff), Wasser und Treibstoff zu und die Zahl der Kollisionen nimmt zu, sodass die Gasphasenkorrosion verstärkt wird.Daher ist die Auswahl eines geeigneten wasserbasierten Gasphasen-Rostschutzmittels sehr wichtig
2) Flüssigphasenkorrosion: Aufgrund der Aktivierung einer erhöhten Konzentration können einige Verunreinigungen (z. B. Wasserstoffionen usw.) in einem schwachen Glied und Verpackungsmaterialien zu beschleunigter Kollision und Korrosion führen, daher sollte die Wahl des Flüssigphasen-Rostschutzmittels sorgfältig abgewogen werden kombiniert mit pH-Wert und Rohstoffen.
3) Grenzflächenkorrosion in Kombination mit Druck, Aktivierungskatalyse, Luft (Sauerstoff), Wasser, Treibmittel, Verunreinigungen (wie Wasserstoffionen usw.) ist eine umfassende Reaktion, die zu Grenzflächenkorrosion führt. Die Stabilität und das Design des Formelsystems sind von entscheidender Bedeutung .

Zurück zur vorherigen Frage: Warum funktioniert der Stabilitätstest manchmal, bei der Massenproduktion gibt es aber immer noch eine Anomalie?Folgendes berücksichtigen:
1: Stabilitätsdesign des Formelsystems, wie z. B. pH-Änderung, Emulgierungsstabilität, Sättigungsstabilität usw
2: Es liegen Verunreinigungen im Rohmaterial vor, wie z. B. Veränderungen der Wasserstoffionen und Chloridionen
3: Chargenstabilität der Rohstoffe, pH-Wert zwischen den Rohstoffchargen, Größe der Inhaltsabweichung usw
4: die Stabilität von Aerosoldosen und Ventilen und anderen Verpackungsmaterialien, die Stabilität der Dicke der Verzinnungsschicht, der Ersatz von Rohstoffen durch den Preisanstieg der Rohstoffe
5: Analysieren Sie jede Anomalie im Stabilitätstest sorgfältig, auch wenn es sich um eine kleine Änderung handelt, und treffen Sie eine vernünftige Beurteilung durch horizontalen Vergleich, mikroskopische Verstärkung und andere Methoden (dies ist derzeit die Fähigkeit, die in der heimischen Aerosolindustrie am meisten fehlt).
Daher umfasst die Stabilität der Produktqualität alle Aspekte, und es ist notwendig, über ein vollständiges Qualitätssystem zur Kontrolle des gesamten Lieferkettenhafens (einschließlich Beschaffungsstandards, Forschungs- und Entwicklungsstandards, Inspektionsstandards, Produktionsstandards usw.) zu verfügen, um den Qualitätsstandard zu erfüllen Strategie, um die endgültige Stabilität und Konformität unserer Produkte sicherzustellen.
Was wir derzeit leider mitteilen möchten, ist, dass Stabilitätstests nicht garantieren können, dass es bei Stabilitätstests keine Probleme gibt, und dass die Massenproduktion keine Probleme haben darf.Durch die Kombination der oben genannten Überlegungen und Stabilitätstests jedes Produkts können wir die überwiegende Mehrheit der versteckten Gefahren verhindern.Es gibt immer noch einige Probleme, die darauf warten, von uns erforscht, entdeckt und gelöst zu werden.Einer der Reize von Aerosolen besteht darin, dass von mehr Menschen erwartet wird, dass sie mehr Rätsel lösen.
Zeitpunkt der Veröffentlichung: 23.06.2022





